Kan uhelbredelig hjernekreft bekjempes med immunterapi?
Forskere er dypt uenige om hvorvidt et nytt legemiddel kan gjøre immunforsvaret i stand til å knekke en veldig aggressiv form for hjernekreft.
Hvert år får rundt 300 nordmenn diagnosen glioblastom.
Det er den mest aggressive formen for hjernekreft, og pasientene lever i gjennomsnitt bare i rundt 14 måneder etter at diagnosen har blitt stilt.
– Det er en forferdelig sykdom. I dag finnes det ikke noen behandling som kan gjøre pasientene friske, sier Walter Fischer, som er tidligere nevrokirurg ved Rigshospitalet i København og en av hovedforfatterne bak en ny studie i det vitenskapelige tidsskriftet Nature Communications.
Han mener den nye studien gir håp om en fremtidig behandling av glioblastom. Ideen er at et legemiddel skal gjøre celler fra immunforsvaret i stand til å kjenne igjen og bekjempe kreftceller.
– Vi tar ut noen av pasientens egne celler i laboratoriet og lærer immunforsvaret å gå til angrep på kreftcellene. Når vi sender dem inn i pasienten igjen, kan vi se at immuncellene finner veien opp til hjernen, forteller Per Guldberg, som er gruppeleder og forskningsprofessor ved Center for Kræftforskning under danske Kræftens bekjempelse. Han er også en av hovedforskerne bak den nye studien.
Stor skepsis fra andre forskere
Flere andre forskere er imidlertid skeptiske til metoden og mener at forskere og leger ikke bør gi pasienter med glioblastom falske forhåpninger.
De påpeker at andre forskningsresultater – som fortsatt ikke er publiserte – tyder på at behandlingen ikke har noen nevneverdig effekt.
– Vi har testet behandlingen på 15 pasienter, men vi avsluttet forsøket fordi behandlingen ikke hjalp dem. Tvert imot, sier Charlotte Aaquist Haslund, som er overlege ved danske Aalborg Universitetshospital.
– I vårt forsøk virket standardbehandlingen bedre, og derfor kunne vi ikke forsvare å fortsette å gi en eksperimentell behandling, legger hun til.
Forskningsprofessor Per Guldberg og det farmasøytiske selskapet CytoVac i Hørsholm, som står bak den eksperimentelle immunforsvarsbehandlingen, er uenige i denne versjonen av forløpet.
Haslund har presentert forsøket på en konferanse, men hun har fortsatt ikke fått skrevet en vitenskapelig artikkel om resultatene. Det innebærer at de negative forsøksresultatene – i motsetning til forsøket i Nature Communications – fortsatt ikke har gjennomgått fagfellevurdering, som er en slags kvalitetssikring der forskningsresultater blir sjekket og vurdert av andre forskere.
Ikke tegn på bivirkninger
Samtidig påpeker Per Guldberg og de andre forskerne bak studien i Nature Communication at den nye immunforsvarsbehandlingen inntil videre ikke viser tegn til å ha bivirkninger.
Og hos tre av de i alt 25 pasientene med glioblastom som inngår i Nature Communications-studien, kunne forskerne se en bemerkelsesverdig forbedring.
Denne forbedringen så nevrokirurg Walter Fischer med sine egne øyne mens han arbeidet som lege og leder av den kliniske delen av studien ved Rigshospitalets Nevrokirurgiske klinikk.
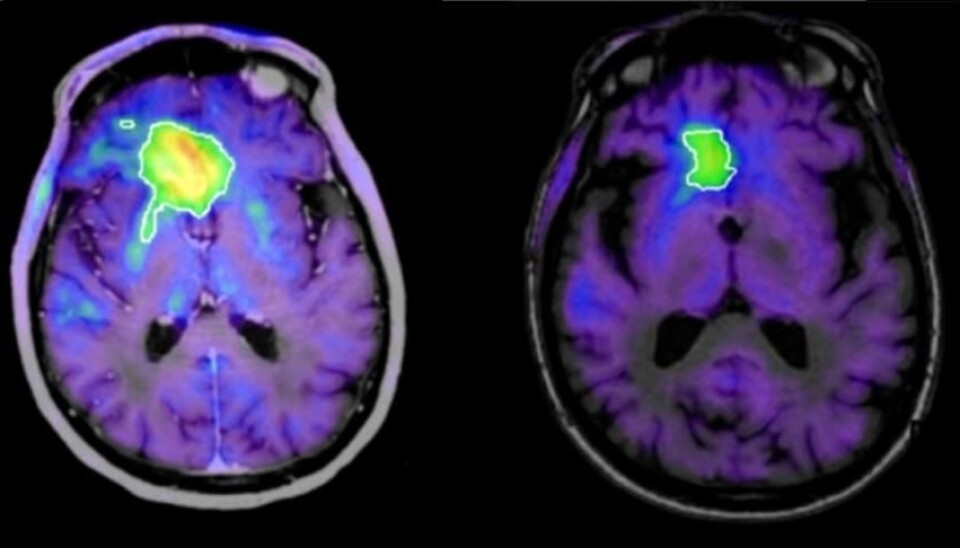
– Vi fikk pasientene til vårt forsøk når de hadde vært gjennom all annen behandling og var gitt opp – det vil si at kreftsykdommen var veldig fremskreden. Den første pasienten var ekstremt syk. Han hadde en enorm kreftsvulst i hodet, og jeg trodde ikke det var noe å gjøre. Jeg tenkte: «Hvis vi kan hjelpe ham, vil det være et mirakel», forteller Fischer, som i dag arbeider som selvstendig forsker.
– Da jeg møtte den samme pasienten fem uker senere, trodde jeg ikke mine egne øyne. Vi skannet hodet, og svulsten hadde begynt å skrumpe. Det øyeblikket vil jeg aldri glemme. Jeg har arbeidet med denne kreftformen i mange år, så jeg vet hvor håpløs den er, legger Fischer til.
Alle pasienter døde
Den første pasienten i forsøket, som var en eldre mann, endte ifølge Walter Fischer med å bli så frisk at han kunne vende tilbake til orkesteret sitt – og pasienten levde mot alle forventninger flere år etter å ha fått diagnosen glioblastom.
Hjernesvulsten kom imidlertid tilbake, og i dag er mannen død, akkurat som alle andre 25 pasientene i studien.
Men forskerne håper at de vil få bedre resultater ved å forbedre metoden og starte behandling tidligere.
– Vi har selvfølgelig bare sett en begrenset effekt på en begrenset del av de 25 pasientene. Men det må sees i lys av hvor alvorlig denne kreftsykdommen er. Bare det å se en effekt har vært helt fantastisk. Det er virkelig mot alle odds, sier Walter Fischer.
– 10 av de 25 pasientene, som inngår i studien, døde før de i det hele tatt rakk å få behandlingen. Så alvorlig var sykdommen.
Reiste seg fra rullestolen
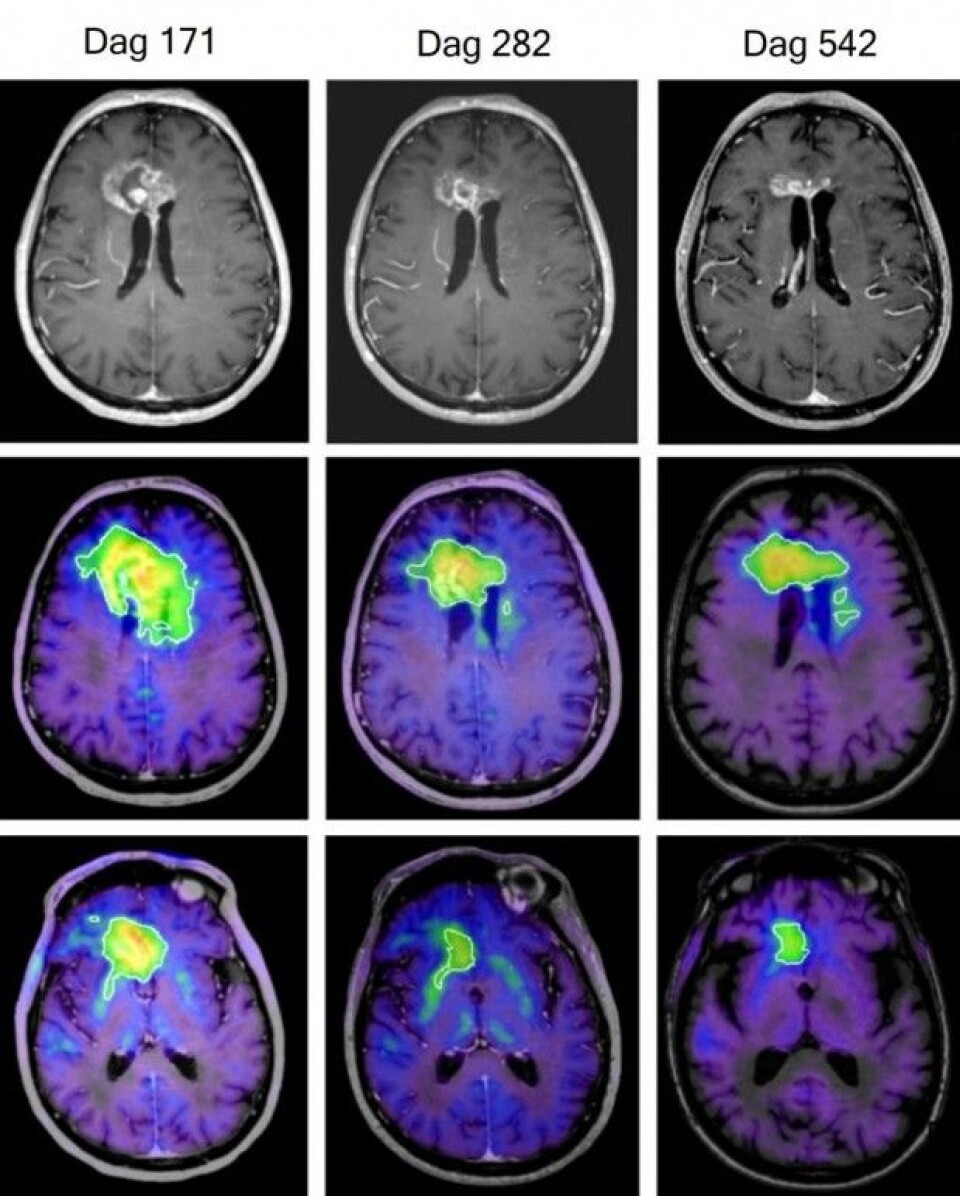
Fischer henviser til at en annen av de tre pasientene var en eldre kvinne som endte med å reise seg fra rullestolen.
Skanninger av hjernen hennes inngår i den nye studien, og de viser at hun ikke lenger hadde tegn på hjernekreft da hun døde.
– Hun levde flere år etter å ha fått diagnosen, og hun døde ikke på grunn av kreft, men på grunn av en annen sykdom. Da man obduserte henne, fant man ingen tegn på kreft i hjernen, sier Fischer.
Enkelthistorier teller ikke
Andre forskere, som ikke har deltatt i studien, understreker imidlertid at man ikke kan legge for mye vekt på disse solskinnshistoriene.
Selv om glioblastom anses for å være en uhelbredelig kreftsykdom, finnes det sjeldne tilfeller der den kan stoppes ved hjelp av standardiserte behandlinger som cellegift, stråling eller operasjoner.
Dermed er det ikke noe epokegjørende i at tre pasienter blir bedre, påpeker hjernekirurg Rene Laursen, som er formann for Dansk Neuro-Onkologisk Gruppe (DNOG) – en tverrfaglig sammenslutning av leger som behandler hjernesvulster.
– Vi har av og til også pasienter der hjernesvulsten plutselig forsvinner med den konvensjonelle behandlingen. Det er antagelig helt tilfeldig at tre av disse pasientene opplevde bedring, sier Rene Laursen, som er hjernekirurg ved Aalborg Universitetshospital og har blitt involvert i utprøvingen av den eksperimentelle behandlingen sammen med Charlotte Aaquist Haslund i det såkalte fase 2-forsøket.
– Jeg skulle inderlig håpe at denne metoden kunne hjelpe pasientene våre, men da vi testet den, viste det seg dessverre at den ikke virket, sier Laursen.
Går ofte galt i større forsøk
Samme holdning har professor Thor Straten, som selv forsker på hvordan immunforsvaret kan bekjempe kreft.
Han påpeker at forsøkene som Charlotte Aaquist Haslund sto i spissen for – og som foregikk etter forsøket i Nature Communications – tilsynelatende ikke viste gode resultater.
– Det er dessverre ikke første gang noe ser virkelig lovende ut når man tester det på noen få pasienter. Men når man senere tester behandlingen i større forsøk, har den plutselig ingen effekt. Man kunne skrive lange bøker om hvorfor det er slik, men det er dessverre skjebnen for mange medisiner, sier Thor Straten, som er direktør for Center for Cancer Immunterapi ved Herlev Hospital i Danmark.
– Jeg har selv arbeidet med utvikling av behandlinger, og det er selvfølgelig virkelig frustrerende når det etter mange års arbeid og store økonomiske investeringer likevel ikke virker. Men slik er virkeligheten noen ganger, og det må man akseptere.
Behandling ble gitt senere
Forskere fra Kræftens Bekæmpelse og CytoVac mener imidlertid ikke at man kan konkludere med at den nye kreftbehandlingen ikke virker på bakgrunn av resultatene fra de upubliserte forsøkene til Charlotte Aaquist Haslund.
I forsøket ble 25 pasienter med glioblastom delt opp i to grupper. 15 pasienter fikk CytoVacs kreftbehandling, mens 10 pasienter fikk standardbehandlingen (kontrollgruppen).
I en intern rapport om forsøket fra CytoVac som Haslund er medforfatter på, og som videnskab.dk har fått tilsendt av Kræftens Bekæmpelse, kan vi lese at pasienter som fikk CytoVacs behandling, klarte seg dårligere enn pasientene i kontrollgruppen. Men forskerne konkluderer med at «det kanskje kan skyldes det faktum» at CytoVacs behandling ble satt i gang 28 dager senere enn standardbehandlingen.
Forskerne fra Kræftens Bekæmpelse og CytoVac mener at forsøket var feil designet, og de påpeker at de 28 dagenes «forsinkelse» kan være en forklaring på resultatene.
Immunterapi er en trend
Thor Straten mener likevel at pasienter med glioblastom ikke bør ha forhåpninger til den nye behandlingen. Men han påpeker likevel at studiens metode er nytenkende og «unik».
Det er snakk om en behandling av typen immunterapi. Det er en behandlingsform som i de siste årene har vært i vinden innen kreftforskning, og blant annet ble kåret til årets vitenskapelige gjennombrudd i 2013 av det anerkjente forskningstidsskriftet Science.
Immunterapi går ut på å styrke immunforsvarets evne til å gjenkjenne og bekjempe kreftceller.
Men det finnes en rekke ulike strategier for å oppnå dette målet – og ulike former for immunterapi retter seg mot ulike deler av immunforsvaret.
Forskerne bak studien i Nature Communications har utviklet en ny metode som tilsynelatende får en spesiell del av immunforsvaret – de såkalte T-cellene – til å gå til angrep på kreftcellene.
Disse cellene kan ifølge forskerne gjenkjenne kreftcellene fordi det finnes noen bestemte proteiner – såkalte cancer testis antigener – på overflaten av kreftceller.
Ros for ideen

Ideen bak metoden får ros fra forskere som ikke har vært involvert i studien.
– De presenterer helt klart en nyhet og en spennende idé. Det er for tidlig å si om metoden vil virke eller ikke, men ideen er unik, sier Tim Elliot, som er professor i eksperimentell onkologi ved det britiske University of Southhampton og professoren i immunterapi ved Cancer Research UK.
Ideen om metoden ble klekket ut omkring år 2005 av ekteparet Alexei Kirkin og Karine Dzhandzhugazyan, som kommer fra henholdsvis Russland og Armenia, men har bodd og forsket i Danmark i en årrekke – og som har vært med på å bygge opp det farmasøytiske selskapet CytoVac i Hørsholm.
– Det er et oppløftende resultat de presenterer i studien, og det er en rask og lett måte å få has på et bredt utsnitt av cancer testis antigener. Men vi må selvfølgelig huske at det er et veldig lite forsøk, så inntil videre vet vi ikke om det vil virke på pasientene, sier Tim Elliot.
– Jeg vil ikke være negativ, men det at behandlingen er personlig og må utvikles til hver enkelt pasient, gjør det også vanskelig å forestille seg at det en dag vil bli en mainstream behandling. Personlige behandlinger er alltid veldig dyre og tidkrevende.
Testet i Sverige
CytoVac og flere av forskerne bak den nye studien påpeker at det kanskje er grunnlag for at metoden kan utvides til andre former for kreft enn hjernekreft.
For tiden gjennomfører CytoVac nye forsøk i Sverige, der firmaet tester immunterapien i samarbeid med svenske sykehus, inkludert Karolinska Universitetshospital. Igjen sikter forsøket mot behandling av den aggressive hjernekreften glioblastom, men denne gang er forsøksdesignet endret.
– Vi vet at immunterapi noen ganger tar litt lengre tid om å virke enn andre former for behandling. Derfor er ideen at vi starter tidligere denne gangen – like etter at pasientene har fått diagnosen, forteller Walter Fischer.
I de pågående forsøkene i Sverige får pasientene immunterapien fra starten og parallelt med vanlig kreftbehandling med cellegift, strålebehandling og lignende.
Normalt å stoppe forsøk
Andre forskere er skeptiske til at CytoVac fortsetter å teste immunterapimetoden selv om Charlotte Aaquist Haslunds forsøk ikke viste positive resultater.
– Det er helt normal prosedyre at man stopper et forsøk hvis man ikke ser noen effekt på de første 10–15 pasientene. Det er fordi man statistisk sett vet at da er det bare en liten sjanse for at behandlingen har en effekt, og da bør man ikke utsette flere pasienter for å teste behandlingen, forklarer Hans Skovgaard Poulsen.
Han er professor og leder av avdelingen for nevroonkologi ved Rigshospitalet og kjenner resultatene fra de upubliserte forsøkene til Haslund.
– Det grunnvitenskapelige i den nye studien er solid. Problemet er bare at forsøkene har vist at det ikke har noen effekt. Det er veldig ergerlig. Det ville være fantastisk hvis et lite, dansk firma hadde klart å utvikle en medisin som kunne hjelpe pasientene våre, men dessverre ser det ut til at det ikke virker, sier Poulsen.
– Det er ikke en mirakelkur
Folkene bak CytoVacs immunterapi ergrer seg over at andre forskere er så skeptiske.
Men Rene Laursen og andre leger ergrer seg over at CytoVac «fortsetter å presse på».
– Det virker som om de lar økonomiske interesser og sin egen tro på behandlingen komme foran pasientene, sier Laursen.
– Hvis dette blir framstilt i media som at vi nå plutselig har fått en mirakelkur mot hjernekreft, så kan mange desperate pasienter og pårørende plutselig få falske forhåpninger. Når de ringer i morgen, er det vi som må forklare dem at det er snakk om en gammel nyhet om en behandling som vi har testet for flere år siden, og som ikke virket.
Referanser:
A.F. Kirkin mfl: «Adoptive cancer immunotherapy using DNA-demethylated T helper cells as antigen-presenting cells», Nature Communications (2018), doi: 10.1038/s41467-018-03217-9
C. Haslund mfl: «An Open-Labelled, Randomized Phase II Study in Patients with Recurrent Glioblastoma Multiforme Comparing Progression Free Survival of Alecsat (Autologous Lymphoid Effector Cells Specific Against Tumour-Cells) Versus Bevacizumab/irinotecan», Neuro-Oncology, vol 18, pp. iv6. DOI: 10.1093/neuonc/now188.017 Sammendrag
«Randomized Phase 2 Study to Investigate Efficacy of ALECSAT in With GBM Measured Compared to Avastin/Irinotecan», 2016, ClinicalTrials.gov
© Videnskab.dk. Oversatt av Lars Nygaard for forskning.no.