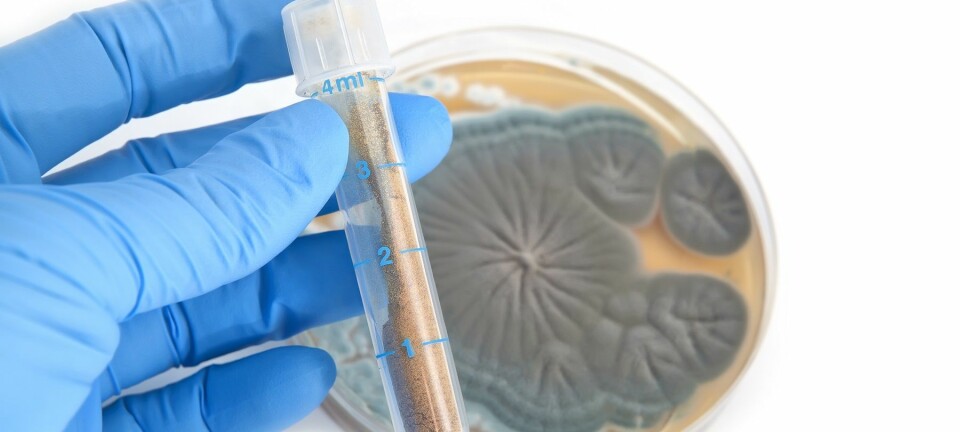
– Vi har designet en gruppe molekyler som bakteriene ikke kjenner igjen fra naturen. Disse molekylene forstyrrer den livsviktige sinkbalansen i bakteriecellen, og dermed også bakteriens evne til å ødelegge antibiotika, forteller Pål Rongved og Alexander Høgmoen Åstrand. (Foto: Ola Sæther)
Vil få antibiotika til å virke igjen
De skulle finne en kur mot kreft. I stedet oppdaget de et stoff som kan ta knekken på resistente bakterier.
I samarbeid med forskningsmagasinet Apollon
Antibiotikaresistens er blitt et enormt helseproblem i verden. Introduksjonen av nye antibiotika på markedet stuper. Det er bare funnet opp to genuint nye antibiotika i løpet av de siste 30 årene. Samtidig blir bakteriene stadig flinkere til å utvikle resistens.
– Bakteriene er de eldste cellene på jorden. Helt siden tidenes morgen har bakteriene slåss mot hverandre og andre mikroorganismer i naturen. De kan fordoble seg på under ett minutt og har derfor store muligheter til å endre seg i senere generasjoner. Kommer vi med et nytt antibiotikum, kan bakteriene snu seg rundt mye raskere enn vi mennesker kan og utvikle en ny, biologisk mekanismene som motvirker det nye antibiotikumet, forteller professor Pål Rongved ved Farmasøytisk institutt på Universitetet i Oslo.
Forstyrrer sinkbalansen
Sammen med postdoktor Alexander Høgmoen Åstrand prøver han å forhindre at resistens utvikler seg så raskt. De er nødt til å tenke nytt.
Mye av antibiotikumet som kommer på markedet, er hentet rett fra en soppkultur eller i jordbakterier som har vært i naturen lenge. Selv om det syntetisk blir gjort små forandringer med antibiotikumet, vil bakteriene fortsatt komme opp med resistens.
– Vi har designet en gruppe molekyler som bakteriene ikke kjenner igjen fra naturen. En av mekanismene til disse molekylene, er at de kan binde seg til sink, også i bakteriene. Da forstyrrer de den livsviktige sinkbalansen i bakteriecellen, og dermed også bakteriens evne til å ødelegge antibiotika.
Åstrand og Rongved jobber med den største klassen av antibiotika, de såkalte beta-laktamantibiotika, hvor blant annet det klassiske penicillinet tilhører. Ved å kombinere disse antibiotiske stoffene med molekylet som forskerne har syntetisert på laben, hemmer det veksten til bakteriene.
– Det syntetiske stoffet vårt ser ut til å eliminere resistensen hos bakteriene, slik at noen moderne antibiotika kan begynne å virke igjen. Klarer vi å motvirke normal sinkmengde inne i bakteriecellene, er vår hypotese at det vil bli vanskeligere for bakteriene å utvikle resistens, sier Åstrand.
Fra kreft til livsfarlige bakterier
Det hele startet med et doktorgradsarbeid om kreft og sink, som de ikke fikk så gode resultater med. Under et kjemiseminar møtte forskerneØrjan Samuelsen fra Universitetssykehuset i Nord-Norge. Samuelsen er sjef for K-res-laboratoriet, som samler alle de nye, farlige bakteriene fra pasienter i Norge – et stort bibliotek med resistente bakterier.
– Vi kom i snakk med miljøet i Nord-Norge og forskere fra Kjemisk avdeling på UiT, og fikk grønt lys for å evaluere stoffene vi forsket på, hos dem, i håp om at det kanskje var mulig å bruke sinkbindere sammen med antibiotika i stedet. Det var da det virkelig begynte å ta av, forteller Rongved.
Forskerne fikk tilgang på et helt bibliotek av kliniske isolater. Og kombinert med antibiotikumet meropenem, gav forskernes eget sinkbindende molekyl gode resultater.
– Meropenem er et antibiotikum som legene sterkt begrenser bruken av. De har det «i skuffen» på sykehuset og sparer det til eventuelle krisesituasjoner, av frykt for at bakteriene skal bli resistente mot det. Medisinen har vært på markedet i omtrent ti år, men bruken er svært begrenset. Man må havne på sykehuset med livstruende sykdom for at det skal bli brukt, sier Rongved.
Når Samuelsen tester dette antibiotikumet på de farlige bakteriene, virker det ikke. Bakteriene er allerede resistente.
– Men da vi tilsatte stoffet vårt, begynte legemiddelet å virke igjen.
Jakten på den riktige dosen
Prosjektet har nå kommet så langt at forskerne ikke er i tvil om at stoffet virker. Nå går de mot en preklinisk fase, hvor de må bevise at det er stabilt, trygt og sikkert.
Neste steg er å teste stoffet ut på levende rotter, i friske, humane leverceller og i kreftceller. Samtidig jobber forskerne hele tiden med å finne det optimale molekylet og den rette dosen. Både for mye og for lite sink er nemlig skadelig for menneskecellene.
– Det var internasjonalt kjente forskere som mente at slike metallbindere ville være farlige overfor våre egne celler – at vi aldri ville få registrert det som et legemiddel. Men giftighet er et dosespørsmål. Derfor har vi testet det på humane celler og har fått svært gode resultater. Vi har også sett at kreftceller, som er mye mer følsomme enn friske celler, tåler å bli utsatt for stoffet i små mengder. At vi nå har funnet et stoff som også våre egne, syke celler tåler, og som virker mot de mest aggressive bakteriene, er svært lovende, sier Rongved.
Forstyrrer balansen
Men når bakteriene er så smarte og dyktige til å utvikle resistens, hvordan kan forskerne da være sikre på at de ikke blir motstandsdyktige mot også dette stoffet?
– Mens vanlig antibiotika vanligvis angriper ett bestemt sted i bakteriecellene, med kun en metode, angriper vi noe som bakteriene er avhengige av flere steder. Reduserer vi sinkkonsentrasjonen i cellene, vil det forstyrre hele balansen. Bakteriene vil kanskje klare å utvikle resistens mot dette stoffet etter hvert, men vi tror det vil ta lengre tid enn det som er vanlig i dag – også fordi vi bruker et syntetisk stoff som ikke bakteriene kjenner fra før, sier Åstrand.
Forskerne gløder av entusiasme og har stor tro på at pasienter en gang vil kunne få nytte av stoffet.
Ofte kan det ta rundt ti kostbare år å utvikle nye medisiner. Men ved sykdommer som er ekstreme, livstruende eller utgjør store helseproblemer, som for eksempel kreft, er situasjonen en annen. Da gir gjerne myndighetene tillatelse til å teste nye legemidler på pasienter tidligere enn normalt.
Det samme vil kunne gjelde medisiner som virker mot resistente bakterier.
– En av grunnene til at resistensproblemet har eksplodert de siste tre til fem årene, er overforbruket av antibiotika i verden. Det er stort behov for nye løsninger. Hvis resultatene våre fortsetter å utvikle seg i riktig retning, tror jeg vi kan teste dette på mennesker innen fem år, sier Pål Rongved ambisiøst.
Denne artikkelen ble først publisert i forskningsmagasinet Apollon.