Byggeklosser for kunstig liv
Det endelige, fjerne målet for Irep Gözen er å bygge en kunstig celle fra bunnen av.
Den lysende blæra på skjermen ser levende ut. Den svømmer som en amøbe. Men den er ikke levende. I alle fall ut fra vanlige definisjoner på liv.
Det vi ser, er et kunstig cellemembran. Irep Gözen har laget det av lipider – fettstoffer, som i matolje eller margarin. Akkurat som når olje frastøtes av vann og danner dråper på vannflaten, slik danner lipidene ei tynn hinne i fuktige omgivelser. Helt av seg selv.
Bygger liv av ikke-liv

Irep Gözen er oppslukt av dette – hvordan ikke-levende materialer helt av seg selv kan oppføre seg som om de var deler av levende organismer.
– Jeg spør meg: Hva kan materialene i cellen gjøre helt på egen hånd? sier Gözen.
Hun startet sine studier i Tyrkia, fortsatte med doktorgrad ved Chalmers tekniske universitet i Sverige og kom fra en forskerstilling på prestisjetunge Harvard-MIT hit til Forskningsparken i Oslo for åtte måneder siden.
På Norsk senter for molekylærmedisin arbeider Gözen videre med å lage byggeklosser for liv av døde materialer. Hun bygger deler som kan bli liv, byggekloss for byggekloss av molekyler.
Disse molekylene er organiske, men har aldri vært levende. Organiske molekyler – som for eksempel metan – finnes over alt i universet.
– Jeg prøver å finne ut hva disse ikke levende materialene gjør med den levende cellen, sier hun.
Feil folding av proteiner
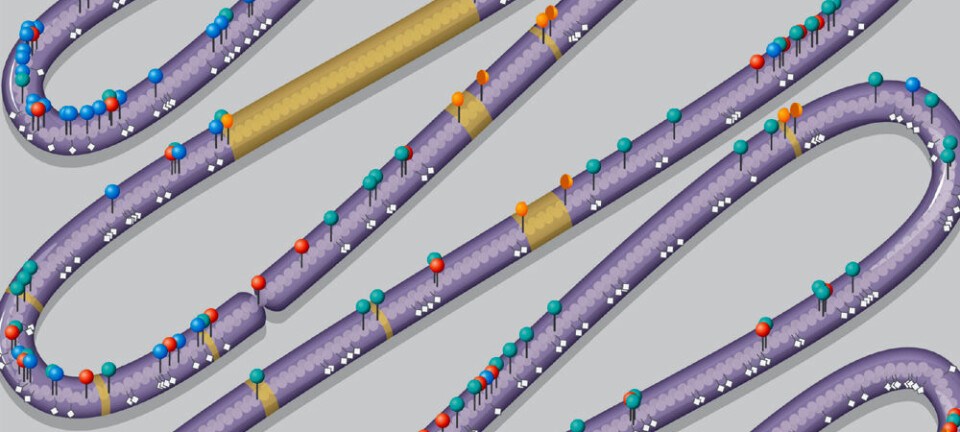
Hennes nyeste kreasjon er første trinn mot en kunstig endoplasmatisk retikulum – E.R. blant venner.
E.R. en av cellens organer, eller organeller, som de kalles. E.R. gjør mye forskjellig. Blant annet hjelper det proteiner å folde seg sammen til den fasongen de trenger for å gjøre jobben sin i kroppen.
Hvis E.R. blir stresset, blir ikke proteinene riktig foldet. Det kan utløse farlige sykdommer som Alzheimer og Parkinsons sykdom eller insulinresistens, som igjen kan gi en form for diabetes.
Å finne ut hvordan E.R. jobber og hvordan det blir stresset, kan altså gi nye måter å bekjempe disse og andre sykdommer på. Gözen er på vei mot en sånn forståelse sammen med kolleger i mange land.
Ett triks om gangen
– I Europa er det flere forskergrupper som arbeider med blant annet kunstige celler, forteller Gözen.
Men før forskerne kan løpe i mål, må de lære å gå. Gözens kunstige E.R. klarer ikke å folde proteiner – ennå.
Den er en forenklet versjon. Den klarer bare å gjøre ett av triksene til en ekte E.R. – å krølle seg sammen. Den bruker heller ikke samme energikilde som den ekte for å krølle seg.
Det er sånn forskerne må jobbe når de vil forstå livet fra bunnen av og opp.
– Jeg konsentrerer meg om bare én egenskap, en adferd. Da kan du klare deg med få byggeklosser, sier Gözen.
To opptak av Irep Gözens forenklede utgave av endoplasmatisk retikulum. Videoene er hentet fra tidsskriftet Biomaterials Science, 2017,5, 1256-1264.
Nedenfra og opp – eller ovenfra og ned
Med disse enkle byggeklossene setter hun og kollegene hennes sammen deler som kan gjøre mer og mer.
Andre forskere starter i motsatt ende. De jobber ikke nedenfra og opp, som Gözen. De jobber ovenfra og ned.
De begynner med levende celler. Så forandrer de ett og ett gen og ser hvordan cellen forandrer seg. På den måten prøver de å trenge dypere og dypere ned i cellens mysterier.
Stopp den cellen!
Mysteriene er mange, både sett ovenfra og nedenfra.
– Vi vet ennå ikke hvordan celler beveger seg. Ruller de på en overflate som en bil på hjul eller kravler de som en larve ved å trekke seg sammen og utvide seg? sier Gözen.
Dette er viktig å få rede på. Kreftceller er blant cellene som beveger seg – sprer seg – i kroppen med alvorlige følger.
Hvis vi forstod hva som setter fart på kreftcellene, kunne vi kanskje klare å stanse spredningen.
– Vi kan tenke at kreftforskning er som et svart hull av kompleksitet, men kanskje er det noe ganske enkelt nedi der som vi kan manipulere, sier Gözen.
Ørsmå hjelpere
Dette er den praktiske nytten av denne forskningen. Viktige medisinske metoder kan komme ut av enkle mekanismer som er inspirert av levende celler.
Slike små biomaskiner kan påvirke for eksempel kreftceller. Eller de kan ta med seg medisiner og levere dem akkurat der de trengs i kroppen.
Forskere arbeider også for å lage kunstige celler som kan erstatte antibiotika.
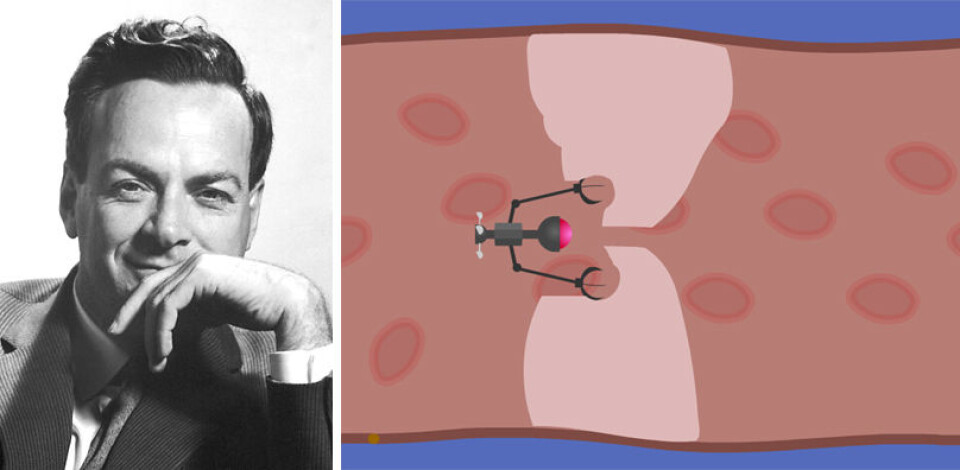
En gang lenger inn i framtida kan slike mekanismer også brukes til ørsmå roboter som reiser med blodstrømmen og gjør inngrep, som mikrokirurger.
Fysikeren Richard Feynman foreslo dette i et foredrag allerede i 1959. Nå – nesten 70 år seinere – arbeider Gözen og mange andre forskere med å virkeliggjøre denne visjonen om å kunne «svelge en kirurg», som Feynman uttrykte det.
Minimal kunstig celle
Men det ultimate målet til Gözen er å sette sammen disse kunstige byggeklossene til noe mer enn små hjelpere.
– Den ultimate drømmen er å lage en minimal celle som kan gjøre det samme som celler med et stoffskifte og evne til å formere seg, sier hun.
Det er langt fram. Materialene hun jobber med er vanskelige å håndtere. Hun trenger komplisert utstyr.
– Jeg kan ikke bare kjøpe utstyr til mikroskopet og så virker det med en gang. Det krever mye innsats, forteller Gözen.
Heldigvis går utviklingen raskt. Ny teknologi – som nanoteknologi – er til hjelp.
Svømmer i salt hav
Og når forsøkene først lykkes, er det spennende materialer hun jobber med. Hva betyr det egentlig at fettstoffer og andre materialer organiserer seg selv og etterligner livsprosesser?
Hva gjør de enkelte materialene i cellen på egen hånd, uten styring ovenfra? Hva gjør cellen ut fra programmeringen i arvestoffet? Kanskje er det vanskelig å skille dette fra hverandre.
Gözen bruker et bilde av en svømmer i et salt hav med mye oppdrift for å forklare. Hvor mye av bevegelsen gjennom vannet skyldes de planlagte svømmetakene og hvor mye skyldes oppdriften i havet?
Svømmetakene er som programmeringen i cellen og oppdriften er hva materialene gjør uten sentral styring.
– Det er overraskende hvor mye materialene gjør for cellen, sier Gözen.
Livet som læremester
Tenker du videre på dette, kan du også spørre: Hvordan oppstod livet på jorda? Var det døde materialers evne til å organisere seg selv om var begynnelsen til den første levende celle?
Gözen og kollegene hennes har livet selv som læremester når de prøver å gjenskape livet nedenfra. Men i dette tilfellet er eleven ganske forskjellig fra læremesteren.
Læremesteren er evolusjonen selv – en blind utvikling uten et bestemt mål. Livet er utviklet gjennom mange små endringer og utvelgelse av de endringene som klarte seg best.
Eleven kan derimot ha sine egne, klare mål for hva hun vil oppnå.
Forbedre livet
Hva om Gözen og kollegene hennes finner nye og bedre metoder enn evolusjonen selv? Kanskje finnes det en mye enklere og mer direkte kurs mot målet enn evolusjonens mangslungne og rotete omveier?
– Det du kaller rotete, kaller vi komplekst. Hvis det er komplekst, er det trolig av en god grunn, kommenterer Gözen.
Likevel har hun tenkt å prøve nye veier mot målet enn de som livet viser henne. Hun planlegger for eksempel å bruke helt andre materialer, en form for plast som kalles polymerer, for å lage byggeklossene til liv.
Mange fag sammen
Gözen er nøye med ikke å overselge sin egen forskning. Det er fortsatt mange små skritt å gå, for henne og kollegene hennes.
Hun jobber svært selvstendig på Institutt for molekylærmedisin. Det er tilknyttet Universitetet i Oslo, men rekrutterer forskere fra mange land.
– Jeg er godt fornøyd med å arbeide i Norge, forteller Gözen.
Her er kort vei fra ett fagfelt til et annet og åpne dører inn til andre institutter. Gözen kan få hjelp av kolleger til å bygge utstyret hun trenger for å avsløre livets hemmeligheter.
– I min forskning er det ikke bare biologi. Du må skjønne kjemi, materialvitenskap og mikrofabrikering, sier hun.
Miljøet er mindre. Derfor er det lettere – og nødvendig – at forskerne samarbeider mer over faggrensene.
– I Boston var det 60 universiteter. Det var helt vilt, sier hun.
Sommerjobben i boks
Selv om Gözen har stor frihet og bra arbeidsforhold, er tempoet høyt og de seine kveldene mange.
– Jeg tar ingen sommerferie, smiler hun.
Referanse:
Bilal, Taylan & Gözen, Irep (2017). Formation and Dynamics of Endoplasmic Reticulum-like Lipid Nanotube Networks. Biomaterials Science. ISSN 2047-4830. . doi: 10.1039/C7BM00227K, sammendrag.